
FRUQUINTINIB VERSUS PLACEBO IN PATIENTS WITH REFRACTORY METASTATIC COLORECTAL CANCER (FRESCO-2): AN INTERNATIONAL, MULTICENTRE, RANDOMISED, DOUBLE-BLIND, PHASE 3 STUDY
Dasari A, Lonardi S, Garcia-Carbonero R, et al. Lancet 2023; 402: 41-53
Il carcinoma del colon-retto rappresenta il terzo tumore più diagnosticato e la seconda causa di morte per cancro nel mondo. Circa il 50% dei pazienti con carcinoma del colon-retto sviluppa metastasi a distanza nel corso della malattia. Il tasso di sopravvivenza a 5 anni per i pazienti metastatici è del 15% e sono scarse le opzioni terapeutiche dopo trattamenti sistemici standard (chemioterapia e terapie a bersaglio molecolare e, nelle linee successive, trifluridina-tipiracil e regorafenib).
Fruquintinib è un inibitore orale della tirosin-chinasi, potente e altamente selettivo dei recettori del VEGF (Vascular Endothelial Growth Factor) di tipo 1, 2 e 3, che sono regolatori chiave dell’angiogenesi associata a crescita tumorale e metastasi. Nella Figura 1 è riportato il meccanismo d’azione di fruquintinib.
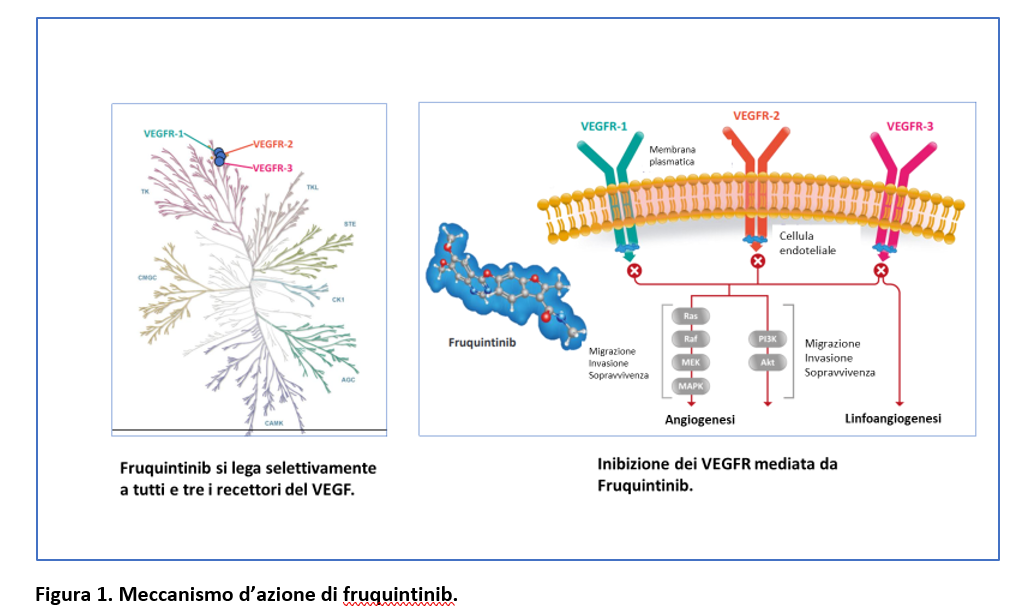
Nel 2018, lo studio di fase 3 FRESCO (LI J. et al, JAMA 2018) aveva randomizzato pazienti con carcinoma del colon-retto metastatico che avevano ricevuto almeno 2 precedenti linee di chemioterapia, a ricevere fruquintinib oppure placebo. i risultati avevano dimostrato un aumento significativo con fruquintinib rispetto al placebo della sopravvivenza globale (OS mediana: 9,3 mesi [95% C.I. 8,2-10,5] vs 6,6 mesi [95% C.I. 0,51-0,83]; HR=0,65 [95% C.I. 0,51-0,83]; p< 0,001) e della Progression-Free Survival (PFS mediana: 3,7 mesi [3,7-4,6] vs 1,8 mesi [1,8-1,8]; HR=0,26; p<0,001).
Questi risultati hanno portato all’approvazione di fruquintinib in Cina nel 2018, ove però le terapie standard disponibili per il carcinoma metastatico del colon-retto erano differenti in quel periodo temporale rispetto al resto del mondo in quanto gli inibitori di VEGF o di EGFR non erano inclusi di routine nel trattamento standard e il regorafenib e trifluridina-tipiracil non erano ancora stati approvati. Nel FRESCO solo il 30% dei pazienti aveva ricevuto precedente trattamento con INIBITORE di VEGF e solo il 14% un anticorpo anti-EGFR e nessun paziente aveva ricevuto trifluridina-tipiracil. Inoltre, i pazienti che avevano ricevuto regorafenib erano stati esclusi (LI J. et al, JAMA 2018).
Uno studio di fase 1/1b ha valutato fruquintinib negli USA in pazienti con carcinoma metastatico del colonretto indipendentemente da precedente terapia con trifluridina-tipiracil o regorafenib. I risultati preliminari incoraggianti erano stati incorraginati in termini di attività antitumorali e tossicità (Dasari A, JCO 2022).
E’ stato quindi condotto uno studio internazionale randomizzato per valutare la efficacia e la tossicità del friquintinib in pazienti affetti da carcinoma del colon-retto metastatici: lo studio FRESCO-2.
METODI
Lo studio FRESCO-2 è uno studio internazionale (condotto in 14 nazioni nel Nord America, Europa, Asia e Australia), randomizzato, doppio ciclo, placebo controllato. Erano elegibili pazienti ≥ 18 anni di età (≥ 20 in Giappone), con adenocarcinoma del colon retto metastatico (istologicamente o citologicamente documentato) che avevano ricevuto tutti i trattamenti standard, compresi chemioterapia con fluoropirimidine, oxaliplatino e irinotecan, terapia anti-VEGF, anti-EGFR (se RAS wild type) e in progressione o con intolleranza a trifluridina-tipiracil o regorafenib. Doveva essere documentato stato di RAS, BRAF e instabilità di microsatelliti o mismatch repair. Pazienti con mutazione di BRAF (V600E) dovevano aver ricevuto terapia con inibitore di BRAF se approvato e disponibile in quella nazione. Pazienti con instabilità dei microsatelliti o mismatch repair dovevano aver ricevuto immunoterapia. Altri criteri di eligibilità comprendevano PS ECOG=0-1, malattia misurabile secondo i criteri RECIST v.1.1, valutata localmente. I pazienti eligibili sono stati randomizzati (2:1) a ricevere FRUQUINTINIB (capsule 5mg) o placebo [OS] una volta al giorno dei 1-21-CICLI ogni 28 die.
Fattori di stratificazione erano:
-precedente terapia (TRIFLURIDINE-TIPIRACIL o REGORAFENIB o entrambi);
-STATO mutazionale di RAS (WILD TYPE vs mutato);
-durata della malattia metastatica (≤18 mesi >18 mesi).
L’end point primario era la sopravvivenza globale (tempo dalla randomizzazione alla morte per qualsiasi causa).
Tra gli endpoint secondari:
-Progression-Free Survival (PFS) definita come tempo della randomizzazione alla prima documentazione di progressione valutata dagli sperimentatori in accordo al RECIST v.1.1 o morte per qualsiasi causa;
-tasso di risposte obiettive;
-durata della risposta;
-tossicità.
RISULTATI
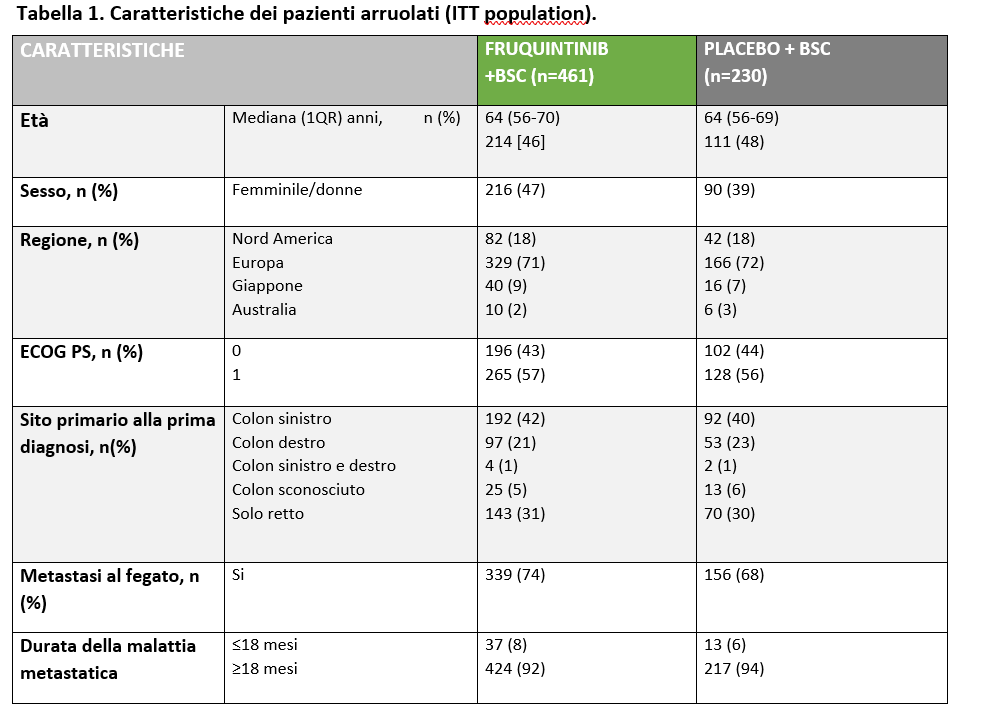
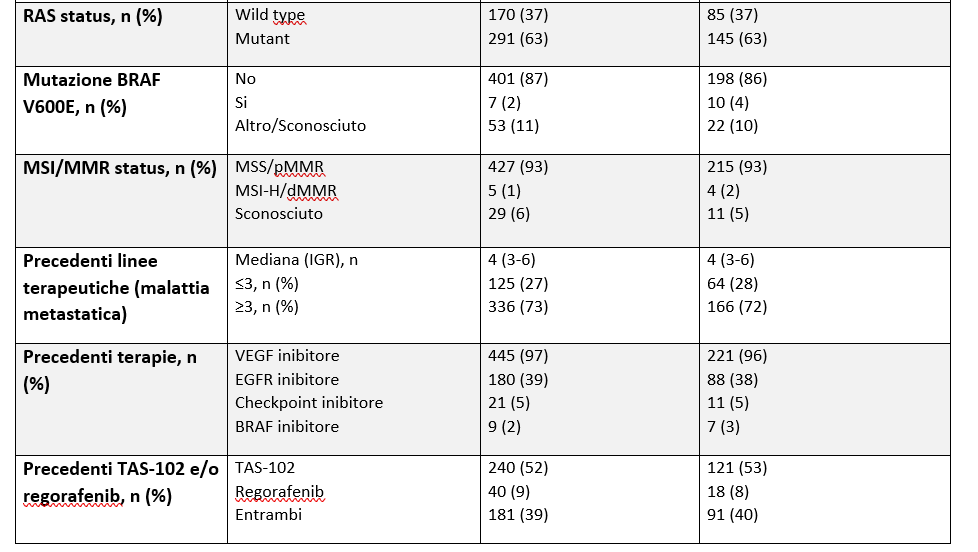
Dall’agosto 2020 al Dicembre 2021 sono stati valutati 934 pazienti e sono stati randomizzati 691 pazienti (R2:1) a ricevere FRUQUINTINIB (=461) o placebo (n=230). Al 24 giugno 2022 (data del cutoff), 20 (4%) dei 461 pazienti del gruppo FRUQUINTINIB e 1 (<1%) del gruppo placebo erano rimasti in trattamento. Nella tabella 1 sono riportate le caratteristiche dei pazienti dell’INTENTION-TO-TREAT (ITT) population. L’età mediana era 64 anni; il 63% dei 691 pazienti randomizzati aveva una mutazione di RAS e il 72% aveva metastasi epatiche. Il 73% dei pazienti aveva ricevuto ≥3 linee di terapia per la malattia metastatica (numero mediano: 4). I tipi di terapia sono riportati nella Tabella 2.
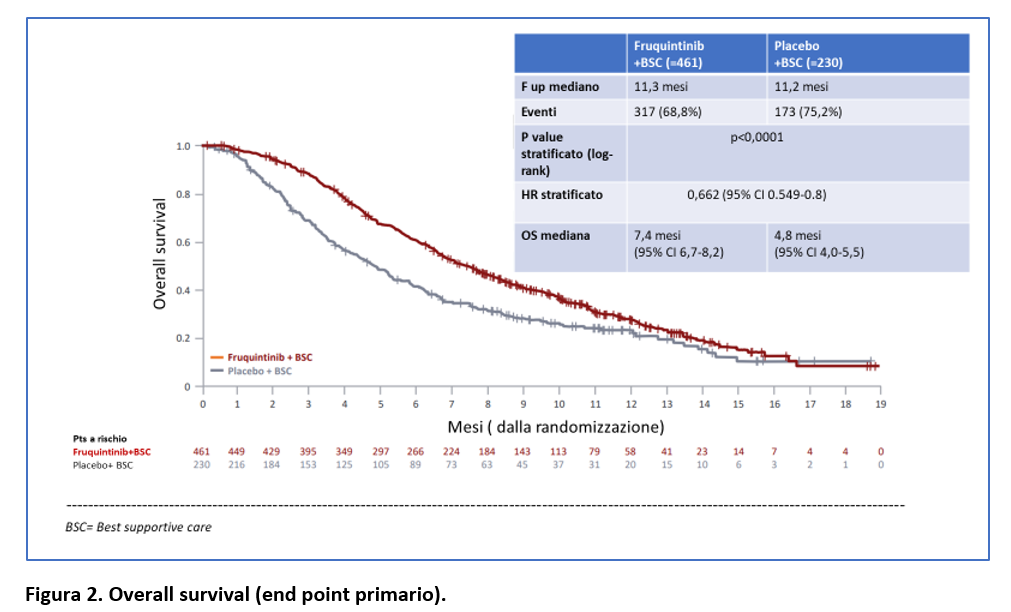
La sopravvivenza globale mediana (end point primario dello studio) è stata di 7,4 mesi (95% CI 6,7-8,2) nel gruppo fruquintinib vs 4,8 mesi (95% ci 4-5,8) nel gruppo placebo, con una differenza in termini assoluti di 2,6 mesi (HR=0,66; 95% ci 0,55-0,80; p<0,0001) (Figura 2).
La proporzione di pazienti ancora vivi a 9 mesi è stata del 41% nel gruppo fruquintinib e del 28% nel gruppo placebo.
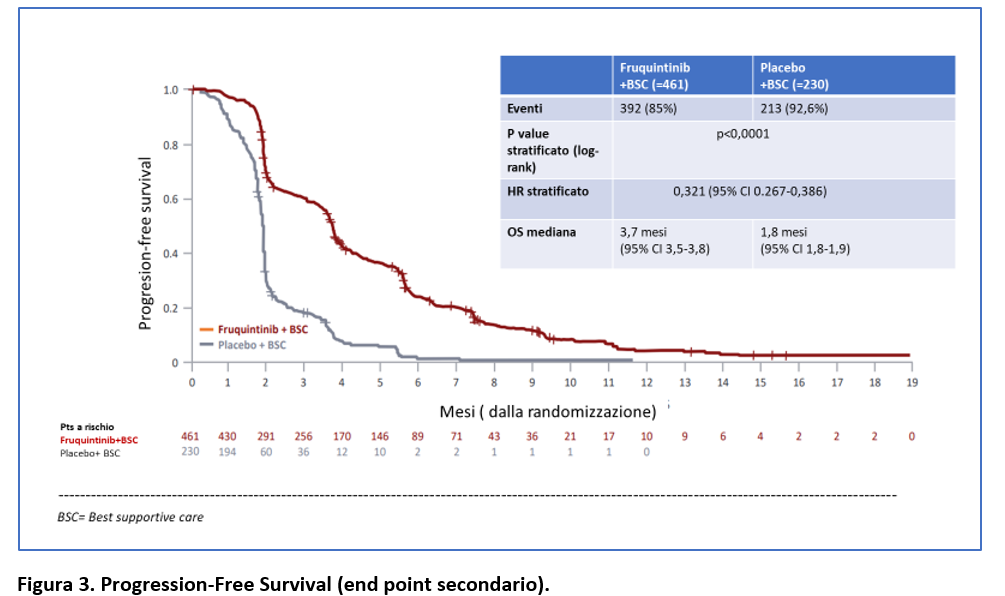
La PFS mediana è stata di 3,7 mesi (95% CI 3,5-3,8) nel gruppo fruquintinib vs 1.8 mesi (95% CI 1,8-1,9) nel gruppo placebo (HR=0,32; 95% CI 0,27-0,39; p<0,0001) (Figura 3).
Le analisi di sottogruppo della OS e della PFS hanno evidenziato risultati consistenti con il beneficio osservato nell’ITT population tra tutti i sottogruppi prespecificati, compresi i fattori di stratificazione alla randomizzazione.
Una risposta obiettiva (valutata dagli investigatori) è stata documentato nel 2% (7/461) dei pazienti del gruppo fruquintinib vs 0% (0/230) nel gruppo placebo (p=0,059). La durata mediana della risposta è stata di 10,7 mesi (Tabella 2).

Gli eventi avversi più frequenti di qualsiasi grado sono stati: ipertensione (37% gruppo FRUQUINTINIB vs 9% gruppo placebo) e astemia (34% vs 29%). Eventi avversi di grado uguale o superiore a 63 sono stati: ipertensione (14% vs 1%) astemia (8% vs 4%) sindrome mano-piedi (6% vs 0%).
CONCLUSIONI
Questo studio internazionale, di fase III randomizzato ha dimostrato che il trattamento con fruquitinib, rispetto a placebo, determina un vantaggio in sopravvivenza globale, end point primario dello studio, e anche in PFS (end point secondario) in pazienti affetti da carcinoma del colon-retto metastatici già sottoposti a più linee di trattamenti standard.
Fruquintinib inoltre è risultato nel complesso ben tollerato pur in presenza di una casistica costituita da pazienti già pretrattati, con interruzioni del trattamento inferiori a quelle riportate da altri studi che avevano arruolato pazienti sottoposti a 3 o più linee di trattamento.
COMMENTO
In Italia, FRUQUINTINIB è attualmente disponibile nell’ambito di un Expanded Access Protocol (EAP) internazionale, supportato da TAKEDA.
BIBLIOGRAFIA
Li J, Qin S, Xu RH, Shen L, et al.
Effect of Fruquintinib vs Placebo on Overall Survival in Patients With Previously Treated Metastatic Colorectal Cancer: The FRESCO Randomized Clinical Trial.
JAMA 2018 Jun 26;319(24):2486-2496. doi: 10.1001/jama.2018.7855.
Dasari A, Hubbard JM, Eng C et al. Phase 1/1b trial of fruquintinib in patients with advanced solid tumors: Preliminary results of the dose expansion cohorts in refractory metastatic colorectal cancer. J Clin Oncol 2022; 40 (suppl 4):93
LINK all’abstract:
https://pubmed.ncbi.nlm.nih.gov/37331369/

