
CLINICAL CHARACTERIZATION OF FGFR2b EXPRESSION IN PATIENTS WITH ADVANCED GASTRIC OR GASTROESOPHAGEAL JUNCTION ADENOCARCINOMA.
Sato S, Rhodes SL, Aoki Y, Nakayama I, Hashimoto T, Hawkins J, Yanes RE, Chang CH, Nakamura Y, Kawazoe A, Mishima S, Kotani D, Kuboki Y, Bando H, Kojima T, Yoshino S, Reading S, Honeycutt H, Finger E, Endo I, Sakamoto N, Kuwata T, Yoshino T, Shitara K.
ESMO Open. 2025 Jul;10(7):105322. doi: 10.1016/j.esmoop.2025.105322
Link all’abstract
https://pubmed.ncbi.nlm.nih.gov/40513139/
OPEN ACCESS
Il recettore FGFR2b (recettore 2b del fattore di crescita dei fibroblasti) è un nuovo biomarcatore proteico espresso nei tumori gastrici e della giunzione gastroesofagea (GC/GEJC). Gli studi di fase III stanno valutando l’efficacia e la sicurezza delle terapie mirate al recettore FGFR2b. Tuttavia, le caratteristiche dei tumori che esprimono FGFR2b e la compresenza dell’espressione di FGFR2b con altri biomarcatori attualmente utilizzabili nel cancro gastrico rimangono poco chiare.
In questo studio di coorte retrospettivo, monocentrico, condotto su pazienti che hanno iniziato una terapia sistemica per tumori gastrici e della giunzione gastroesofagea avanzati, sono state valutate le caratteristiche dei tumori FGFR2b-positivi, i trattamenti di prima linea ricevuti e la coesistenza con alcuni altri biomarcatori utilizzabili a fini terapeutici; HER2, stato del mismatch repair, PD-L1, claudina-18.2.
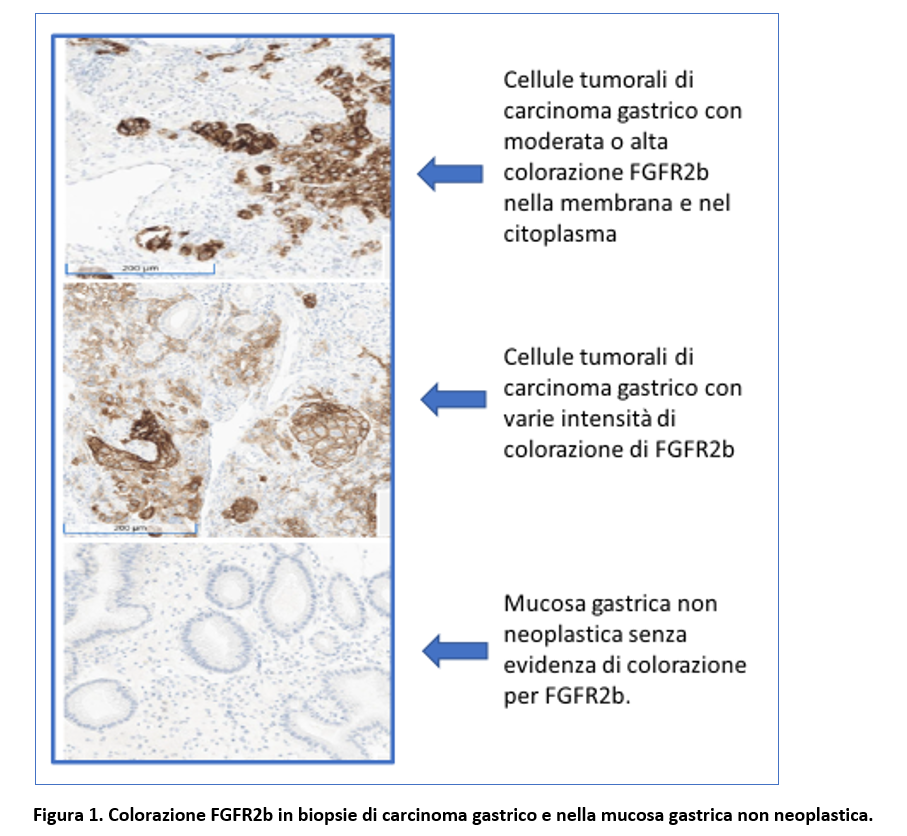
Un campione tumorale è stato considerato FGFR2b-positivo quando sono state rilevate cellule tumorali (>0%) che presentavano una colorazione moderata (2+) o forte (3+) della membrana (Figura 1).
Gli altri biomarcatori sono stati valutati sulla base delle attuali linee guida cliniche.
La sopravvivenza globale (OS) stratificata in base al FGFR2b è stata stimata utilizzando i modelli di regressione proporzionale di Kaplan-Meier e Cox.
Risultati
Dall’aprile 2017 ad ottobre 2024 sono stati identificati 547 pazienti con tumori gastrici e della giunzione gastroesofagea avanzati: 492 (89,9%) avevano i criteri di inclusione/esclusione, presentavano una colorazione FGFR2b valutabile e disponevano di dati clinici completi.
La prevalenza di FGFR2b 2+/3+ era del 15,4% (95% CI: 12,4%-19,0%) nell’intera coorte di pazienti e del 29,8% (95% CI: 22,0%- 38,7%) nei pazienti con campioni raccolti entro una anno e mezzo dall’inizio dello studio.
La maggior parte (53,9%; 95% CI: 42,1%-65,5%) dei campioni tumorali FGFR2b 2+/3+ era negativa per altri biomarcatori.
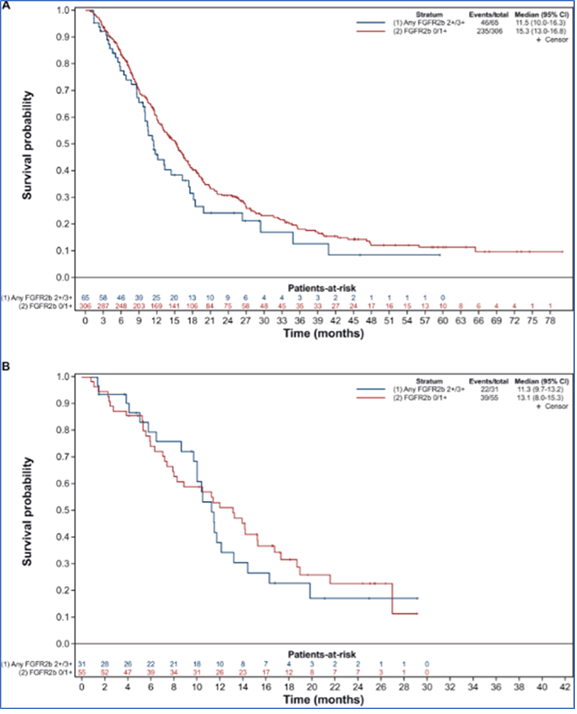
Nei pazienti HER2-negativi trattati in prima linea con sola chemioterapia, la mediana della sopravvivenza globale era di 11,5 mesi (95% CI 10,0-16,3 mesi) per pazienti con colorazione di FGFR2b 2+/3 e 15,3 mesi (95% CI 13,0-16,8 mesi) per pazienti con colorazione di FGFR2b 0/1+ (Figura 2).
Non è stata riscontrata alcuna associazione tra il livello di sovra-espressione di FGFR2b e la sopravvivenza globale (HR=1,14; 95% CI,84-1,55).

Commento
Questo studio ha rivelato una limitata sovrapposizione della sovraespressione di FGFR2b con i biomarcatori attualmente utilizzabili, nella pianificazione terapeutica del carcinoma gastrico e della giunzione gastro-esofagea avanzato, suggerendo che FGFR2b è un nuovo biomarcatore che identifica una popolazione distinta di pazienti affetti da GC/GEJC che potrebbero trarre beneficio da una terapia mirata a FGFR2b.
Un’altra informazione importante derivante da questo studio retrospettivo è relativa alla più bassa percentuale di FGFR2b positivi evidenziati in campioni collezionati da oltre una anno e mezzo: questa informazione era stata data per altri biomarcatori e gli studi clinici in corso richiedono oggi campioni freschi o tessuti d’archivio ottenuti da non oltre 6 mesi prima dell’arruolamento per la valutazione centralizzata di FGFR2b (Rha 2025; Wainberg 2022; Smyth 2022).
Bibliografia
Rha SY, Zhang Y, Elme A, et al. Prevalence of FGFR2b protein overexpression in advanced gastric cancers during prescreening for the phase III FORTITUDE-101 trial. JCO Precis Oncol. 2025;9:e2400710.
Wainberg ZA, Cutsem EV, Moehler MH, et al. Trial in progress: phase 1b/3 study of bemarituzumab þ mFOLFOX6 þ nivolumab versus mFOLFOX6 þ nivolumab in previously untreated advanced gastric and gastroesophageal junction (GEJ) cancer with FGFR2b overexpression (FORTITUDE-102). J Clin Oncol. 2022;40(suppl 16):TPS4165.
Smyth EC, Chao J, Muro K, et al. Trial in progress: phase 3 study of bemarituzumab þ mFOLFOX6 versus placebo þ mFOLFOX6 in previously untreated advanced gastric or gastroesophageal junction (GEJ) cancer with FGFR2b overexpression (FORTITUDE-101). J Clin Oncol. 2022;40(suppl 16):TPS4164.

