
LORLATINIB VERSYS CRIZOTINIB IN PATIENS WITH ADVANCED ALK-POSITIVE NON-SMALL CELL LUNG CANCER: 5-YEAR OUTCOMES FROM THE PHASE III CROWN STUDY
Benjamin J. Solomon, et al.
J Clin Oncol 2024 May 31:JCO2400581. doi: 10.1200/JCO.24.00581
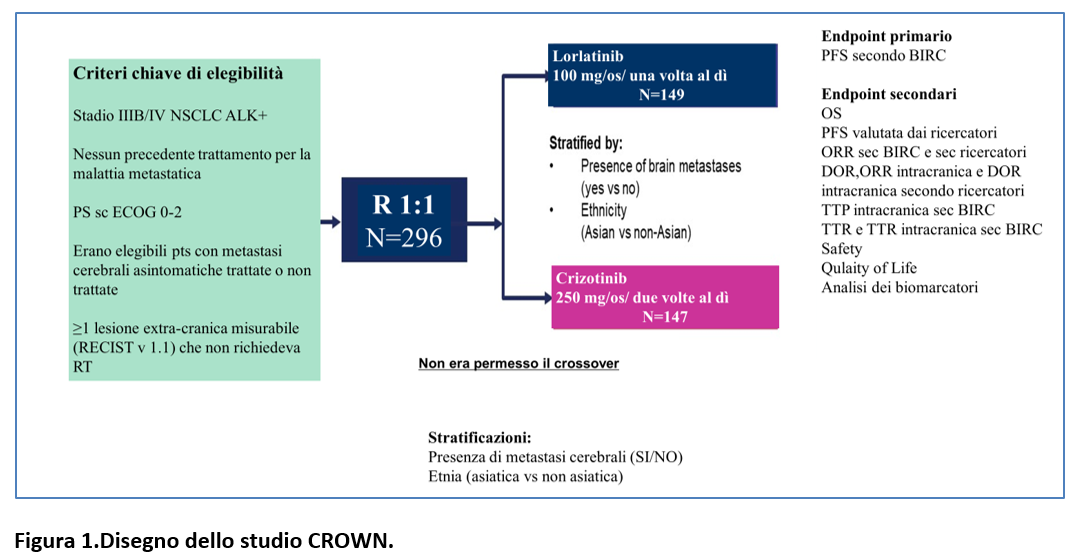
Lo studio CROWN di fase 3, randomizzato, internazionale, open-label, ha confrontato lorlatinib (ALK TKI di terza generazione) versus crizotinib in pazienti non pretrattati con NSCLC avanzato ALK-positivo (Figura 1).
I pazienti erano stati randomizzati (1:1) a ricevere ricevere lorlatinib 100 mg/os/ una volta al giorno (n=149) oppure crizotinib 250 mg/os/due volte al giorno (n= 147) in cicli della durata di 28 giorni.
L’endpoint primario era la PFS valutata dal BICR (sec RECIST v1.1). Endpoint secondario chiave era la sopravvivenza globale (che doveva essere valutata alla seconda interim analisi specificata dal protocollo, dopo almeno 139 decessi). Altri endpoint secondari includevano: la PFS valutata dai ricercatori; la risposta obiettiva; la risposta obiettiva intracranica, ecc (Figura 1).
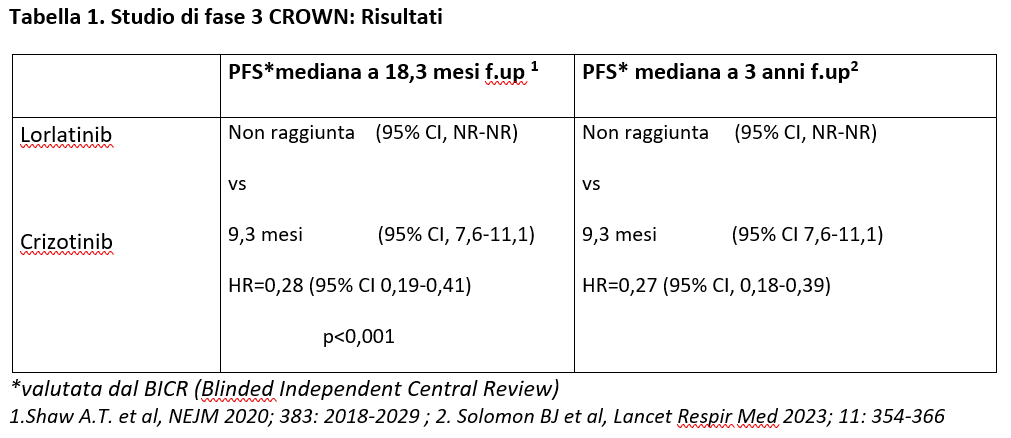
Lo studio ha dimostrato di aumentare in maniera statisticamente e clinicamente significativa la PFS rispetto al crizotinib, sia all’analisi ad interim pianificata a 18,3 mesi di follow up (Shaw A.T. et al., 2020) sia alla successiva analisi post-hoc a 3 anni di follow up (Solomon BJ et al., 2023) (Tabella 1).
In questo articolo vengono riportati i risultati dell’analisi post hoc condotta dopo 5 anni di follow up, relativi a:
-PFS valutata dai ricercatori;
-safety;
-analisi dei biomarcatori (Figura 2).
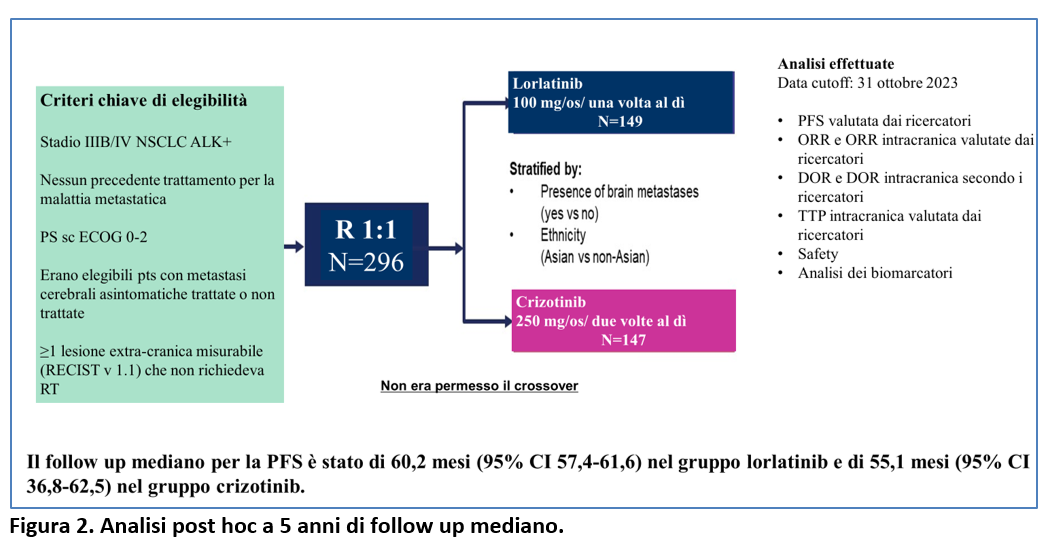
Poiché l’obiettivo primario dello studio (PFS valutata dal BICR) era stato raggiunto all’analisi ad interim prespecificata a 18,3 mesi di follow-up mediano (Shaw AT et al, 2020), in questa analisi post hoc a 5 ani di follow up mediano non è stato pianificata una ulteriore analisi comparativa della PFS per protocol e non è stato fatto un test formale statistico.
RISULTATI dell’analisi post hoc a 5 anni di follow up mediano
Alla data del cutoff per questa analisi (31 ottobre 2023), 74/149 (50%) dei pazienti trattati con lorlatinib e 7/142 (5%) dei pazienti trattati con crizotinib stavano continuando a ricevere il trattamento previsto. Con un follow-up mediano per la PFS di 60,2 per lorlatinib e 55,1 mesi per crizotinib, la PFS mediana non è ancora stata raggiunta (95% CI, 64,3-NR) nel gruppo lorlatinib ed è di 9,1 mesi (95% CI, 7,4 -10,9) nel gruppo crizotinib (HR= 0,19; 95% CI, 0,13-0,27).
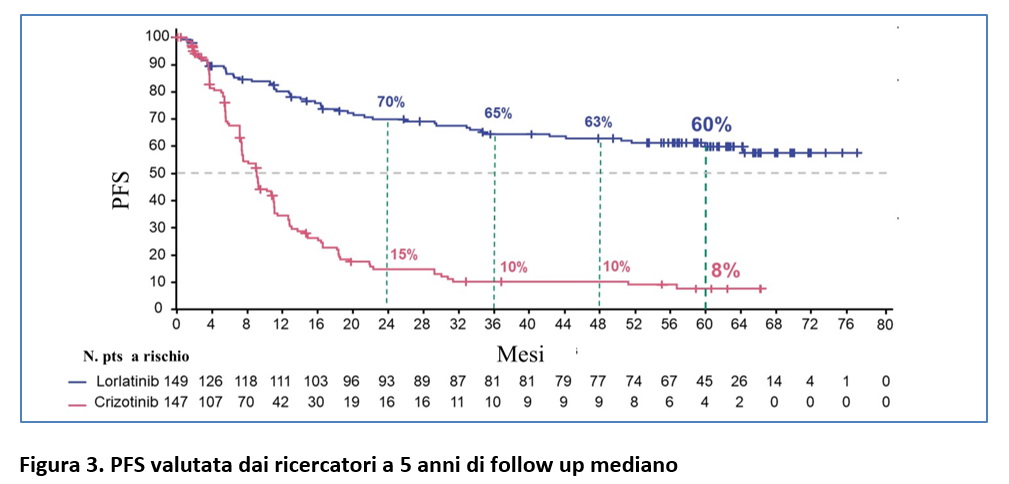
La PFS a 5 anni è pari al 60% (95% CI, 51-68) nel gruppo lorlatinib e all’8% (95% CI, 3-14) nel gruppo crizotinib (Figura 3).
Nella Tabella 2 sono riportati i tassi di risposte obiettive confermate dai ricercatori, i tassi di risposte obiettive intracraniche nei pazienti con metastasi cerebrali al basale (misurabili e/o non misurabili) e il tempo alla progressione intracranica valutata dai ricercatori.
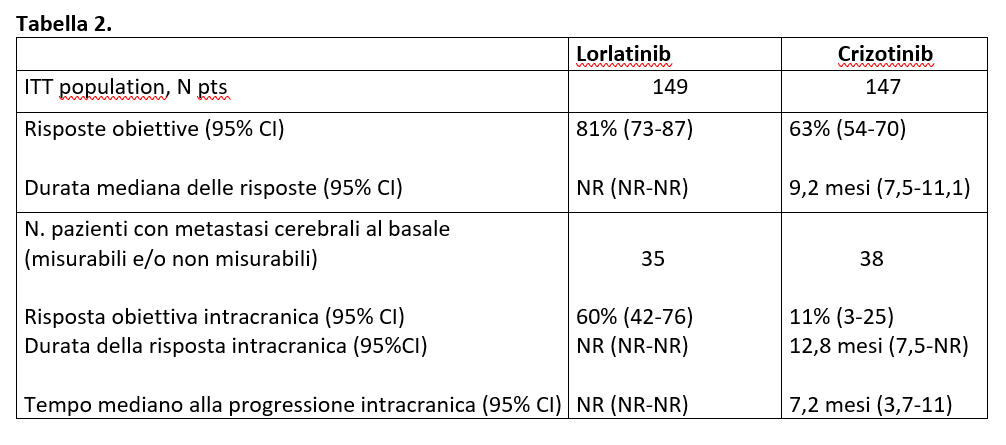
Tra i pazienti con metastasi cerebrali al basale (misurabili e/o non misurabili; n=35 nel gruppo lorlatinib e n=38 nel gruppo crizotinib), la PFS non è stata raggiunta (95% CI, 32,9-NR) con lorlatinib mentre è stata di 6 mesi con crizotinib, (95% CI, 3,7-7,6), con HR=0,08 (95% CI 0,04-0,19).
Tra i pazienti senza metastasi cerebrali al basale, la PFS non è stata raggiunta nel gruppo lorlatinib (95% CI, 64,3 mesi-NR) ed è stata di 10,8 mesi (95% CI, 9-12,8) nel gruppo crizotinib (HR= 0,24; 95% CI 0,16-0,36).
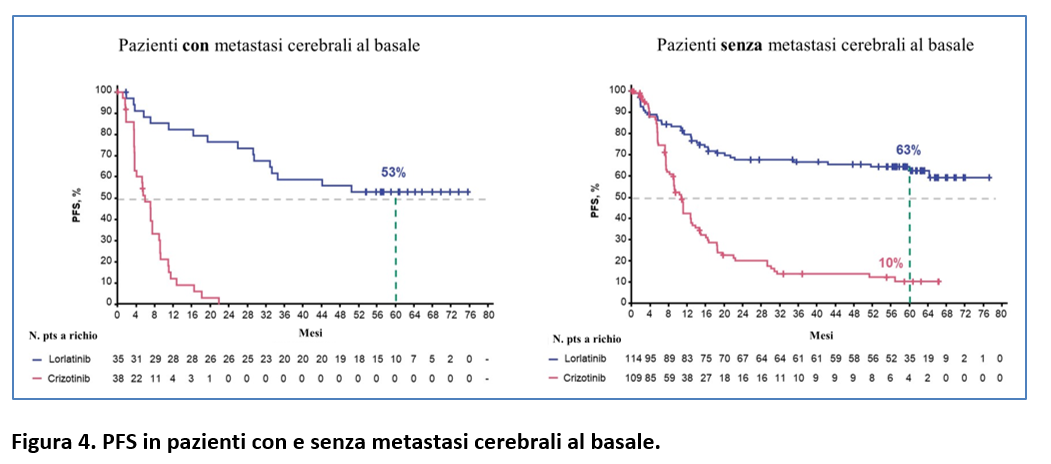
Nei pazienti senza metastasi cerebrali al basale, la PFS a 5 anni è stata del 63% (95% CI, 52-71) con lorlatinib e del 10% (95% CI, 5-18) con crizotinib (Figura 4).
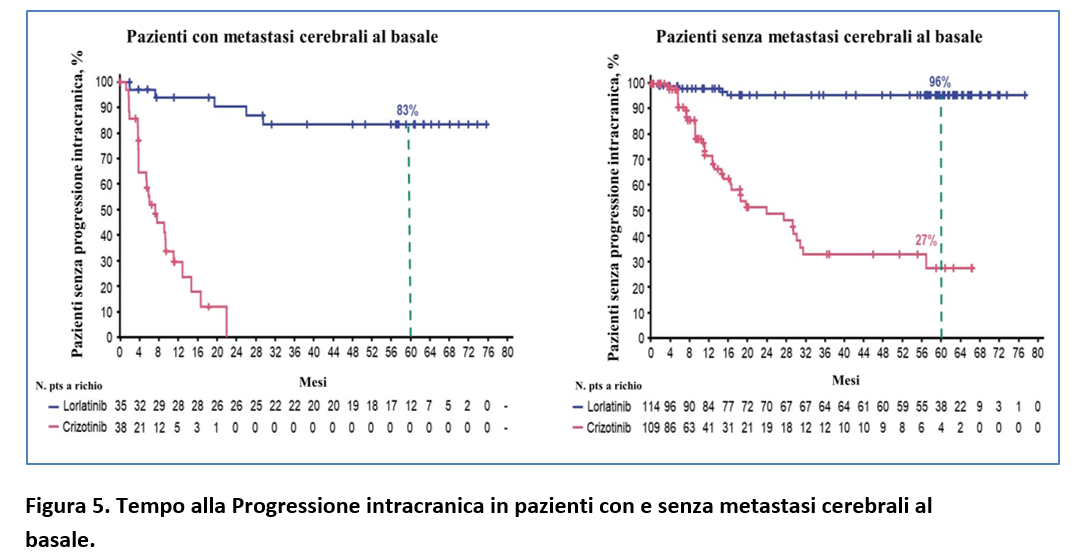
Nei pazienti con metastasi cerebrali al basale, la probabilità di essere liberi da progressione intracranica a 5 anni è stata dell’83% con lorlatinib (Figura 5) mentre nei pazienti senza metastasi cerebrali basali, il 96% di quelli trattati con lorlatinib non aveva sviluppato a 5 anni di follow up metastasi cerebrali vs il 27% di quelli trattati con crizotinib (Figura 5).
SAFETY
Non sono state riportate nuove tossicità. Ad una post hoc analisi, la dose riduzione di lorlatinib effettuata nelle prime 16 settimane non ha impattato sulla PFS mediana né sul tempo alla progressione intracranica.
ANALISI DEI BIOMARCATORI
Al termine del trattamento erano disponibili campioni di ctDNA per 31 pazienti del gruppo lorlatinib e 89 del gruppo crizotinib: nuove mutazioni di resistenza di ALK sono state evidenziate alla fine del trattamento con crizotinib ma nessuna alla fine del trattamento con lorlatinib.
CONCLUSIONI
Dopo 5 anni di follow up, la PFS mediana non è ancora stata raggiunta nel gruppo lorlatinib: questo risultato rappresenta la più lunga PFS mai riportata con qualsiasi singola terapia a bersaglio molecolare nel NSCLC. Inoltre, è stata evidenziata con lorlatinib una prolungata efficacia intracranica, senza nuovi dati di tossicità.
COMMENTO
I risultati a 5 anni di follow up dello studio CROWN sono stati presentati all’ASCO 2024 da Solomon BJ e sono stati contemporaneamente pubblicati nel Journal Clinical Oncology.
Per ulteriori approfondimenti, collegarsi al video del POST-CHICAGO 2024 di AIGOM ed ascoltare la relazione del Dr Ettore d’Argento:
https://www.aigom.it/2024/06/18/le-novita-da-chicago-2024-17-giugno-2024-ore-15-00-18-00/
BIBLIOGRAFIA
Shaw AT, Bauer TM, de Marinis F, et al: First-line lorlatinib or crizotinib in advanced ALK-positive lung cancer. N Engl J Med 383:2018-2029, 2020
Solomon BJ, Bauer TM, Mok TSK, et al: Efficacy and safety of first-line lorlatinib versus crizotinib in patients with advanced, ALK-positive non-small-cell lung cancer: Updated analysis of data from the phase 3, randomised, open-label CROWN study. Lancet Respir Med 11:354-366, 2023
Link all’abstract
https://pubmed.ncbi.nlm.nih.gov/38819031/


